מדללי דם: שיטת חישוב חדשה למניעת סיבוכים
חולים שנזקקים לתרופה קומדין, למניעת קרישי דם וטיפול בהם, עוברים דרך ארוכה ואף מסוכנת עד למציאת המינון הנכון עבורם • שיטה חדשה שפיתחו חוקרים מ20- מרכזים רפואיים בעולם, כולל צוות מהדסה בירושלים, תאפשר לכל רופא לחשב את כמות התרופה המדויקת שהחולה צריך לקבל
אחת הבעיות הניצבות בפני רופאים שרושמים קומדין לחולים שלהם היא למצוא את המינון המתאים, שימנע מצד אחד את תופעות הלוואי הפוטנציאליות הקשות שלה, ומצד שני יאפשר להם ליהנות מיתרונותיה ללא סיכונים מיותרים. אך האתגר הזה קשה במיוחד: המינון ה"נכון" הוא בעל טווח רחב מאוד, בגלל שוני בתגובות הפיזיולוגיות של אנשים שונים לתרופה. יש חולים שחצי מ"ג של התרופה ביום ידלל את דמם לרמה הרצויה, בעוד אחרים זקוקים ל30- עד 40 מ"ג ביום כדי להגיע לאותה תוצאה.
עד היום נהוג היה להתחיל במינון ממוצע ולעלות למינונים גבוהים (או לרדת לנמוכים) יותר תוך כדי טיפול וביצוע בדיקות דם תכופות להערכת רמת הדילול של הדם. נוסחה חדשה, שפותחה לאחרונה על ידי חוקרים מ20- מרכזיים רפואיים בעולם, בהם צוות מהמחלקה לפרמקולוגיה קלינית במרכז הרפואי הדסה בירושלים, תאפשר מעתה התאמה ראשונית טובה בהרבה של התרופה לכל מטופל, תוך חיזוי התגובה האישית שלו למדלל והפחתת הסיכונים הנלווים לטיפול למינימום.
תרופה טובה עם שם רע
התרופה קומדין (וורפארין) היא נוגד קרישה המשמש למניעה ולטיפול במגוון של מחלות המגבירות את הסיכון ליצירת קרישים בכלי הדם, בדרך כלל באזורים שבהם זרימת הדם איטית יחסית, כמו בגפיים התחתונות. קרישי דם שנוצרים באזורים אלה עלולים להינתק ממקומם ו"לנדוד" לאזורים אסטרטגיים בגוף, כמו הריאות, שם הם עלולים לחסום כלי דם ריאתיים ולגרום למוות. התרופה משמשת גם למניעת היווצרות של קרישי דם בלב בעת פרפור חדרים ולמעבר של הקרישים האלה למוח, שם הם עלולים למנוע אספקת דם לאזורים חיוניים (שבץ מוחי) ולגרום לנכות קשה ואף למוות.
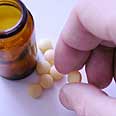
המינון יכול לעלות בחיי אדם. מדללי דם (צילום: ליקוויד)
קומדין נמצאת בשימוש יותר מ50- שנה, ועד היום יש לה מעט מאוד מתחרים. "התרופה הזו החזיקה מעמד עשרות שנים, כי היעילות שלה מאוד טובה," אומר פרופ' יוסי קרקו, ראש היחידה לפרמקולוגיה קלינית בהדסה. "החולים מפחדים ממנה כי יש לה שם רע, שלא בצדק. זו אולי ההזדמנות לציין שראש הממשלה לשעבר אריאל שרון לא פיתח דימום מוחי בגלל הקומדין, אלא בגלל תרופה אחרת".
השם הרע של קומדין נולד, בין השאר, בשל מסלול ההתאמה המפרך של התרופה לחולה שזקוק לה. "כשאתה עומד בפני חולה שזקוק לקומדין, אתה בעצם לא יודע לאיזו קבוצה הוא שייך," אומר פרופ' קרקו. "המינון הרצוי עבור החולה יכול לנוע ממינון מזערי של מיליגרם אחד ליום ועד מינון גבוה מאוד של 20 מ"ג ליום ויותר. עד היום נהוג היה להתאים את התרופה למטופל בשיטה של ניסוי וטעייה, לתת לחולה מינון מסוים ואז לבדוק את מידת הדילול של הדם ולתקן את המינון שוב ושוב, עד שמגיעים לתוצאה הרצויה. ההליך הזה ארוך ולא נותן שום ערובה שהתרופה עושה את שלה, כי במהלך הדרך יש הרבה פעמים קפיצות מסוכנות של ערכי הקרישיות של הדם למעלה ולמטה.
"הבעיה השנייה היא שכל סטייה קטנה מהטווח הטיפולי הרצוי לחולה מסוים עשויה להיות בעלת משמעות עצומה. אם אדם מקבל מינון קטן מדי, הוא נמצא בסכנה לפתח קריש דם חוזר שעלול לסכן את חייו. ואם הוא מקבל מנה גדולה מדי, הוא בסיכון גדול לסבול מדימום, שיגרום לאותה תוצאה עגומה.
"בגלל הבעיות הללו, התאמת התרופה לחולה שזקוק לה הייתה עד היום בגדר 'כאב ראש' לרופא, והרבה רופאים נמנעו מרישום קומדין לחולים שזקוקים לה כדי להימנע מהסכנות האלה. יש ספרות רפואית ענפה המתארת אילו תמרונים הרופאים עושים כדי להימנע מרישום קומדין למטופלים שלהם".
האפקט הגנטי
בשנים האחרונות הצליחו חוקרים ברחבי העולם לחשוף אחדים מהגורמים הגנטיים שמסבירים את התגובה השונה של אנשים שונים לקומדין. בין השאר התגלו שני גנים שמסבירים מדוע חולה אחד עשוי להגיב למינון של חצי מ"ג ביום בלבד, בעוד חולה אחר נזקק לכמויות ענק כדי להגיע לערכי המטרה.
הגן הראשון אחראי על ייצור החלבון שמפרק את התרופה בגוף. ישנם חולים שמסיבות גנטיות החלבון הזה פחות יעיל אצלם בפירוק הקומדין, ולכן הם נזקקים לכמות פחותה מהתרופה, לעומת חולים שמייצרים כמות נורמלית של אותו חלבון. התגלית הזו הביאה לפיתוחה של בדיקה גנטית לזיהוי שינויים בגן, שסייעה בחיזוי כללי אילו חולים יגיבו לכמויות קטנות של התרופה ואילו יזדקקו לכמויות גדולות יותר שלה.
"ערכנו מחקר שנמשך שלוש שנים והשתתפו בו 200 חולים שהגיעו לבית החולים ונזקקו לקומדין לראשונה בחייהם. החולים חולקו לשתי קבוצות: האחת קיבלה את התרופה בשיטה הישנה של ניסוי וטעייה, והשנייה לאחר ביצוע הבדיקה הגנטית והתאמת התרופה לממצאיה," מספר פרופ' קרקו. "ממצאי המחקר הוכיחו כי השימוש בבדיקה הגנטית יעיל ומאפשר לצפות מראש באופן כללי איזה חולה זקוק ליותר תרופה ואיזה לפחות. השימוש בבדיקה הזו איפשר לנו להגיע לערכי המטרה מהר יחסית ובלי קפיצות גדולות".
לפני כמה שנים התגלה גן נוסף, שאחראי על ייצור החלבון שתפקידו לשחזר את מאגרי הוויטמין המסייע בקרישת הדם. גם את הגן הזה ניתן לבדוק כיום במעבדה. בדיקת שני הגנים הללו מניבה 30 קומבינציות גנטיות המנבאות סוגי תגובות שונים לקומדין, והיא שיפרה את היכולת לנבא איזה חולה יזדקק לאיזה מינון של התרופה.
לפני שנתיים הוחלט לאחד את המאמצים העולמיים לפיצוח השוני בין החולים לתגובה לקומדין, והוקם תאגיד בינלאומי לקבוצות מחקר שעסקו בתרופה. כל קבוצה תרמה את הידע שצברה עד אז בנושא, והוקמו קבוצות עבודה
שעסקו בעיבוד היבטים שונים של המחקר החדש. המידע עבר אנליזות שונות ויצר נוסחה מהפכנית, שתאפשר לחזות מראש, ברמה גבוהה של ודאות, איזה חולה זקוק לאיזה מינון של התרופה וכיצד יגיב אליה. התגלית החדשה, שהחוקרים מקווים שתיצור מהפכה של ממש בטיפול בקומדין, פורסמה לפני שבועיים בכתב העת הרפואי "ניו אינגלנד ג'ורנל אוף מדיסין".
"המשוואה שיצרנו מיועדת לרופא המטפל ככלי ראשוני ויעיל לאבחון מינון הקומדין הנדרש לכל חולה," אומר פרופ' קרקו. "היא כוללת פרטים דמוגרפיים על אודות החולה, גילו, משקלו, גובהו, ההיסטוריה הרפואית שלו ומידע על שני הגנים שמשפיעים על דרך הפעולה של הקומדין בגוף. עיבוד הפרטים האלה לתמונה אחת נותן דרגת דיוק גבוהה מאוד לגבי מינון התרופה שיש לרשום לחולה".
הנוסחה לקביעת מינון הקומדין הנדרש תעלה בעתיד הקרוב לאינטרנט, ואף שהיא מיועדת לרופאים היא תאפשר למעשה לכל אדם הנזקק לתרופה להעריך בעצמו לאיזה מינון הוא זקוק. "כדי לקבל את התוצאה המדויקת צריך לדעת את תוצאות הבדיקות הגנטיות, שלא מבוצעות עדיין בשגרה לכל חולה," אומר פרופ' קרקו, "היכולת הזאת קיימת בהדסה, ואנו מקבלים פניות מרופאים וחולים לבצע את הבדיקה וכך לקצר את תהליך ההתאמה של התרופה".
 לפנייה לכתב/ת
לפנייה לכתב/ת